4. uzdevums
74,25 grami cinka nitrāta kristālhidrāta satur 27,00 gramus ūdens. Aprēķini kristālhidrāta formulu!
Atrisinājums
a) Nezināma kristālhidrāta formulu pieraksta Zn(NO3)2·xH2O, kur x parāda, cik molu ūdens satur dotais kristālhidrāts uz katru molu bezūdens sāls.
Tālāk
b) Aprēķini bezūdens sāls masu kristālhidratā.
m(Zn(NO3)2) = m(Zn(NO3)2·nH2O) – m(H2O) = 74,25 – 27,00 = 47,25 g
Tālāk
c) Aprēķina bezūdens sāls daudzumu kristālhidratā.
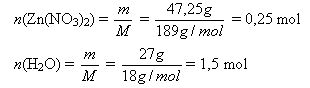 Tālāk
Tālāk
d) Lai noteiktu kristālhidrata formulu, aprēķina, cik molu ūdens ir saistīti ar vienu molu bezūdens sāls.
Ar 0,25 moliem Zn(NO3)2 saistīti 1,5 moli ūdens.
Ar 1 molu Zn(NO3)2 saistīti x moli ūdens.
Tālāk
f) Uzraksta kristālhidrāta formulu.
Zn(NO3)2·6H2O