4. uzdevums
Kopā salēja 200 ml 0,1M bārija hlorīda šķīduma un 100 ml
0,1M nātrija sulfāta šķīduma. Aprēķini reakcijā radušos nogulšņu masu! Kuri joni palika šķīdumā pēc reakcijas?
Atrisinājums
b) Aprēķina uzdevumā doto vielu daudzumus molos pēc formulas n = cV, šķīdumu tilpumus izsaka litros.
100 ml = 0,1l
n(BaCl2) = 0,2 l ∙ 0,1 mol/l = 0,02 mol
n(Na2SO4) = 0,1 l ∙ 0,1 mol/l = 0,01 mol
Tālāk
c) Nosaka reaģējošo vielu un radušos nogulšņu daudzuma attiecības.
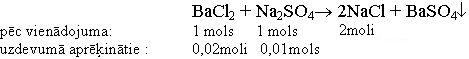
Tālāk
d) Aprēķina, cik molu BaCl2 izreaģē ar 0,01 molu Na2SO4; nosaka, kura no reaģējošām vielām ir pārākumā.
BaCl2 + Na2SO4→ 2NaCl + BaSO4↓
1mols 1mols
n moli 0,01mols
n (BaCl2) = 0,01 mols
Secina, ka BaCl2 ir pārākumā un šķīdumā paliks Ba2+,
Cl- un Na+
joni.
Tālāk
e) Aprēķina nogulšņu daudzumu pēc Na2SO4 daudzuma.
(Nogulšņu daudzumu var aprēķināt pēc izreaģējušā BaCl2 daudzuma!)

n (BaSO4) = 0,01 mols
Tālāk
f) Aprēķina nogulšņu masu pēc formulas m = n ∙ M( BaSO4).
m (BaSO4) = 0,01 moli ∙ 233 g/mol = 2,33 g